�hı�Ͳz�P�w������ ���A��
�w��㦳�J�g�٥B���ħ֪��u�աA�O�@���ȱo�s�x���R����ǡC���H�۰w��B�V��ڤơA��v�b�ϥΰw��ɡA���Ϯڤ��媺�g���ǻ��~�A�]�����Ҽ{��{�N��Ǫ��ѭ�ǡB�Ͳz�ǡB�B�ʾǡB�ͪ���ǵ��]���A��Ƥ�����Ǫ����ѡA�~���n�a���s�w��o������Dz���N�C
�ثe�{�ɤW�A�k�h�ʯe�f�̵M�O�w�몺�D�n�A���g���@�C���孫�I�ĭz�hı��槪���A�����Q�hı���Φ��B�ǻ��B�M�ջs�L�{�A�ä��аw��ϥΡu�����t�Ρv���h����z�C
�@ �hı������
�k�h���������¯ٮɴ���ĵ���H���A�Ͼ��騳�t�a�@�X�k�פ����A���P�D�����Y���ˮ`�A�O�ͩR�L�{�����i�ίʪ��@�ثO�@�ʾA���覡�C�k�h���{���i������譱�A�@�O���P�W���A�t�@�O��m�ѧO�W���C�e��������N�k�h�P�����w�����c���g���A�ò��ͻ����Ӹg��������A���������ǽT����X�h������m�A�H�K���t�@�X�����A�O�@����K�A���S��M�`�����A��ֶˮ`�C
�{�N��ǻ{���A�k�h�ëD�S���Pı�A�]���@����ӭM���`����E�A�p���O�L�j�B�ūL���]45 �ץH�W�^�ιL�C�B�G�k�ʤƾǪ��赥���A�ҥi��_�hı�C�Z����hı�����g����A���i�٬��u�ˮ`�ʨ��Ǿ��v�C�ֽ��M��L��´���ˮ`�ʨ��Ǿ��ҬO�@�عC���λr�S���g����A�o�ǻr�S���g����s���_�ֽ��L�h�ϩM���餺���Y�Dz�´�A�Ѧp�����B���`�n���M�������C�j������Ŧ��´���Ȧ��ֳ\�hı���g���餧���G�A���o�Ǽs�x���G����´�A�@������l�ˤ��୫�[�_�Ӧb�Ϯg�ϳ�_�k�h�C
�ް_�k�h����E�@�Υ]�A�ۿ�����������z�]���M�ƾǦ]���C²��Ө��A����@������I�ǡA���O����ʡB�ƾǩʡB�ΧN���ʪ���E�A���|�]���ت��z��q���ܤƦӤް_��´���s�A���A�γy���ˮ`�A�η|�Φ��@�ؼ��ʪ��ˮ`���A�b��ᦳ�o�Ͷˮ`���i��C���龹�x��´��o�ǯ�q���ܡA�Ҳ��ͪ��۹�����A��U�����O���@�˪��A�����ܱӷP�A�����h���M�A�åB�|���߲z�]���Ҽv�T�C�q�Ͳz���פW�A����P�h���H�ȨèS���t���A�����´��کμ�b�ˮ`�Ҥ��c���P�h���誺�ӷP�ס]��Y��k�h���Ԩ��{�ס^�A�h�|�H�ۭ��骺���|�g���B�߲z���A�M�V�m���]���ӧ��ܡC
�G ���g�ֺ�
���餺���U����T�O�z�L���P����ŶǤJ���g�ֺ��t�d�Ǿɪ��C�ھگ��g�ֺ������c�P�Ͳz�S�ʡA�i�N��Ϥ������P���O�G
A�\�D�n�ǻ�����P�������g�ֺ��A�ñ���٦ת��i�O�ΤϮg�@�ΡA��hı�ǻ��N�q���j�C
A�]�����|�j�B�����T������ʷP�����g���A��ˮ`�ʨ�E���_���������g�ֺ��A����Q�@��L�`��E�ұҰʡA�pIJı�B���O�M�_���A���̼s�x���G�b�ֽ��B�٦סB���x�M���`���A�t�d�������IJı�M�N�ѩʥ���ı�A�����b��U����s���_�@�ΡA�b�hı���ո`�W�A�禳���n�@�ΡC
A�_�O�������|�B�����T���ǤJ���g���A�s�x�s�b�_�֤U�Φ٦ײ�´�A�D�n���ɨ�h�]�Ĥ@�h�^�A�]�٧ֵh�C���t�d�ǻ��㦳���T�d��A����ɶ��u�����U�h�A�Ͼ��騳�t�����M�`�C
C���O���|�p�B�L���T�����g�ֺ��A�B��`�h��´�����C�����ɨ`�h�]�ĤG�h�^�A�κٺC�h�A��k�h�S�I�O�d���T�A����ɶ������w�h�A�]�i����H�۫߯��g�Ϯg�α��P�]���^�ܤơA�Ͼ���ɦV���ʪ��A�A�H�קK�A���ˮ`�C
�T �����ǻ��G
�����ǻ���1965�~�ѱ���]Melzack�^�M���]Wall�^���Ǫ̩Ҵ��ҡA�ܤ����M�g�L�h�����q�A�������W�L�j�ܲ��A�i�ΥH�����D�n���k�h�P��h����C�������p�U�]���Ϥ@�^:
�������ǻ����{���A�hı�ջs���p�h���@�ˡA����۵hı���ǤJ�C�h���}�һP�_�A���M����ֺ�(A�])�P���ֺ�(A�_�MC)���g���۹ﬡ�D�{�סC�hı�@��g��C�����ֺ��ǤJ�A�����|�ɦV�}�ҹh���A���U�hı��T���~��ǿ�[1]�F�խY��E�[�ѩ�Ӧ۸��ʪ����g���A�h�i��P�@�ϰ�Ψ�L�a�϶ǨӪ��h�T�����H����C��Y�O���A���ֺ��ǤJ�ɦV�����h���A���_�hı��T���ǻ��C���{�H�S�p�ڭ̼������˰ϰ�i�y��hı�A�K�O�������ǻ������A�Q��A���ֺ����g���ǤJ�A�h����C���ֺ����hı�ǤJ�@�ΡC���~�A�Ӧۤj���ֽ�ǨӤ��T���A�]�A�U�غ믫���ʤα��P�]�����^�ΰO�е��{���A��i�H��hı�A�p�B�ʭ��b�M�`���ɮɨ��ˡA�ä�ı�o�k�h�A���L�ݤ��ɫ�l���h�P�C
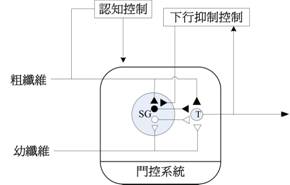
�Ϥ@ �����t�ΥܷN��
�| �hı���ǻ�
1 �hı����
�ˮ`�ʨ��Ǿ��M�G����U��´���A�s�x�����G�b�P���U�����A�䤤�H�ֽ��B�����B���`�B�p��ީM��Ӧ�ޮǵ��l��´���t�������K�סC
�hı�����͡A�D�n�O����l�ˡA�ɭP�������P���ܤƩM�ƾǪ��誺���c�C�o�ǤƾǪ���@�Ωg�ֺ��A�Φ��q���ܤơC���q��F��@�w�{�סA�K���ͽİʡA�g����I���ջs��W�Ǩ쯫�g���ϡC�W�Ǫ���T�A�i�z�L�I���M�d�ǻ��ˮ`�ʨ�E�����g���A�ǰe�찪�쯫�g���ϡA�N�Ѭ��h�P�C
2 ����ǻ�
����I���̨䯫�g�ӭM�ǩʽ�A�i�Ӥ���6�Ӥ��P���h�A�b�\�h���m�����X�A����I�����h�A�]�N�O�Ĥ@�h�M�ĤG�h�B�A���j������A�_�MC��ŶǤJ�ֺ��ǤJ���誺�פ�B[2-4]�C�ˮ`�ʰT����A�_��C�����g�ֺ��ǤJ�A�����I�����h�A���hı�ǻ����|������C���������_�I�A�����W�Ǩ�U�C���z�@����Pı���ְϡA�H�Y�Ǧܤj���ֽ���Pı�ϡC
�h�P���ǻ��b�I���h���A�ѩ���h�譱���]���v�T����o�����C��@�OC���ֺ������A�����F���c��P����~�A�٤��c��L���g����A�p�\���Q�i�B�ѥV����Q�B���t����]������B �M�@��ƴᵥ�A�o�Ǫ���ﯫ�g�ֺ��㿳�ħ@�ΡF��G�O�A��C���MA�_�����g�ֺ����ۧ@�ΤU���������t�Ρ��A��b�I���h���o���@�ΡF��T�O���F�U�檺�ջs���g��b���h���A�����؝�A���IJ�e�ὤ�����ͧ���@�ΡC
3 ���챵��
�j���ֽ�O�t�d��k�h�ʽ誺�����A�åB��T�a�����w���C�j���ֽ�èS���@�ӱ����h�P���M�ϡA�M�ӵhı�����s�����N�q���j�A�����M�o�A�챡�P�M�欰�A�G���ˮ`�ʸ�T�︣�����P���c���|���ͼs�x�v�T�C
������C�������q�ﰼ�ᨤ�W��A������g��C���A�i�Ө�F�j���Pı�ϡA��hı�P���W�_���n�@�ΡC�C���O�j���ֽ�U���Pı�ո`���ߡA���F�t�d�N�Ҧ��Pı��T�Ǩ�j���ֽ誺�Pı�ϥ~�A��_���pô�U�C���M�����鵥���c���@�ΡC�U�C�����}���֤��c�]-���؝�A�O�����w�����h�@�Ϊ����n�����A�Ӥ��c�˵ǤW���ֽ�E���h��ܪ��@�ΡA���U�v�����ݤ����`�����g���A�����ĪG�A��i�z�L�C�W(2-4Hz)���j�q�w����[5]�C
��������������q�����ǤW��A�פ��C���D�S���ָs�A�Ѧ��V�W�s�x��g��j�����s�X�ϡ��Ρ���t�t�Ρ����A�]�A���a�^�A�����ΤU�C���A�@�ί�ް_���m�B�k�פ����A��~�P��E�ʥF���T�������g���Y�A�üv�T�۫߯��g�A�Ʀܤް_���r�ֵ������ܤơC
4 �U��ջs���|
�k�h������A��k���M�I�B�Ұ_�ۭ��n�N�q�C�]���A����b���ı����hı���P�ɡA���Ƥ@�ػP�ͭѨӪ��hı�ջs��O�A�H���P���~�|�ջs�k�h�P���t�ΡC
���줤�ϧ����ֺ��pô��hı�Ǿɳq�����U�ӳ���A�i��U��ʽջs�B�Χ��ܷP���ϰ쪺�j�p�A�ΨϦh�P���ʯ��g����Y�طPı���ǤJ���S���ʪ�����@�ΡC�������ɤ��ޡ��P��ǽ誽���P�I�����g�ζ����q�L���_�ֻP�I�����g���pô���A���i�b�h�P�ǻ��_�ջs�@�ΡC���F�����������c���������_�j�֡A�O����5-�m���i��(5-HT)���g���������a�F�[�WA�_ (IIIb)�i���ıҰʡu���_�j�֡Я���v���U�����t�ΡA����ˮ`�ʸ�T���ǻ�[6]�A�O�w��g�`�Ұʪ��@�Ψt�Τ��@�C
�U�����t�άO��������n���k�h�ӫإߪ����n�\��A��l�ت��O�Ȯɵνw�k�h�A�H�K�����k���M�`�A��������B��C�ʯk�h���A��A��������]�|��h[7]�C
�� �w������
�w�����h��@���z�O��E���Ǿ��A�z�L���骺�ǤJ���g�ֺ��i�J����A�P�Ӧۯk�h���쪺�ˮ`�ʫH���b����h�o�ͬۤ��@�ΡA�g�L����I���������t�Χ@�ΡA��W�Ǫ����g���_����@�ΡC
�@��Ө��A��Ŧ����������A�A���Ӧ�C���ֺ��Ǿɪ��ˮ`�ʨ�E�C�w�����h�v���ɡA�θ�������k�H�Ұʲʯ��g�ǤJ�ֺ��A�K�i�b������ǡA����C�����ֺ����ˮ`�ʨ�E�~��W�ǡA���ͨ}�n�����h�����C�o�خ����i�b����k�h�w�B����A�ϥΧC�j�ר�E�Ӳ��͡C�������o�ͦb�ۦP�ά۪�`�q����X�@�ΡA�i��O���ު����z�̾ڡC
�@��H���m�ֳt���i�w�ޥ��B���w���w���k�B�ξA�����q��E(���W�v50-200Hz�C�j��)�A�����i�H��E���ֺ��]A�]�BA�_, IIIa�^���ǤJ���g���o��F�Ϥ��A�©�͵w���N�A�e�������̱a�Ӥ����n����ʨ�h�A�ҿE�o���O���ֺ����g(C�BA�_,IIIb)�C
���~�A�z�L��E���骺A���ǤJ���g�A���ļv�T�P�@�`�q����P���g����[8-9]�A�q�Ӯ����k�h�Τ@�t�C�����`���Ӫ����g�����A�F��v���ĪG�C����s��ܡA�ϥΧC�W���j�ת���E�ιq�w��E�A�i�ɤJA�]��E�A���oNAD�������c�A�W�j����I���P�`�q����P���g���ʡF�ӧC�j�ת��w��ηL�h�ǤJ�A�h�i��z�P�`�q����P���g����[10]�C�q�L�ձ��Ӫ����g�t�ΡA�i�v����Ŧ�ް_���h���C�ƹ�W�A����DzΨϥΪ�����ީҦb���B�A�����״I����P���g���G�A�G�����e���P����P���g����[11]�A�w�뻷�ݻP�w�B�ۦP�`�q������A�i��E��P���g�@�ΡA�o�����t�ӱj�O�����h�ĪG�C�Ҧp�X�\�B��T1��q���椺���١A�i�E�oT1�q����P���g�ǽ谼���A�q�ӧ��ܩ��Y�V����ۦP�`�q����P���g���ʡA�O�G���f���X�\���������A��{�N��ǭ�z�C�ȱo�@�����O�A�w����P���g�t�Ϊ��@�ΡA�i�H�O�W�j�δ�z�A���Ө��l��´�����ɪ��A[12]�A�o���O������Dzΰw�몺�ۦV�v�����ѤF���ҡC
��Ҥ��Y
[1]
Baldry PE.A Review of Low-Power Laser
Pain-Relieving Controlled Clinical Trials [J]. Acupuncture in Medicine. 1993, 11: 1-10
[2]
Light AR, Perl ER.Spinal termination of functionally identified primary
afferent neurons with slowly conducting myelinated
fibers [J]. J Comp Neurol. 1979, 186: 133-150
[3]
Swett JE, Woolf CJ. The somatotopic organization of primary afferent terminals in
the superficial laminae of the dorsal horn of the rat
spinal cord [J]. J Comp Neurol. 1985, 231: 66-77
[4]
Lu Y, Perl ER.
Modular organization of excitatory circuits between neurons of the spinal
superficial dorsal horn (laminae I and II)[J]. J Neurosci. 2005, 25: 3900-3907
[5] Han. J.S. and Terenius, L., Neurochemical basis
of acupuncture analgesia [J]. Ann. Rev. Pharmacol Toxicol. 1982, 22: 193-220.
[6] Basbaum A, Field H. Endogenous pain
control mechanisms: review and hypothesis [J]. Annals of Neurology. 1978, 4: 451-462
[7] Campbell JN.Mechanisms
of neuropathic pain [J]. Neuron. 2006, 52(1): 77-92
[8] Koizumi K, Brooks C. The spinal cord and the autonomic
nervous system. In:Davidoff (ed) Handbook of the spinal cord
[J].
[9] Oosterndorp R, Functionele
vertebrobasilaire insufficientie[M]. [academic
thesis].
[10] Sato A, Sato Y, and Schmidt
RF. The Impact of Somatosensory Input on Autonomic
Functions [J]. Rev Physiol Biochem Pharmacol. 1997, 130: 1-328.
[11] Bekkering R and van Bussel R. Segmental Acupuncture [M]. In J. Filshie
& A. White. Medical Acupuncture: A Western Scientific Approach. Churchill
Livingston. 1988, p105-136
Sato A, Sato Y, Schmidt RF. The Impact
of Somatosensory Input on Autonomic Functions[J]. Rev Physiol Biochem Pharmacol.
1997,
130: 1�V328
�@��²���G���A�� ����w�b�Ƿ|�z�ʨơF�|�߭���w�b�ǰ|�ư|��
�n�����j�ǰw���t�դh�F���U���z�v���v�C